当前位置:课程学习>>第六章>>课前准备>>本章导学
◆本章概览
一、学习目标
 1、学习启普发生器的工作原理和使用方法
1、学习启普发生器的工作原理和使用方法
 2、 掌握气体的发生、净化等基本原理和操作方法
2、 掌握气体的发生、净化等基本原理和操作方法
 3、学习理想气体状态方程式和阿伏加德罗定律
3、学习理想气体状态方程式和阿伏加德罗定律
二、本章要求掌握的重点:
 1、启普发生器的使用
1、启普发生器的使用
 2、电子天平的使用
2、电子天平的使用
 3、6 mol/L HCl溶液的配置
3、6 mol/L HCl溶液的配置
(本节课要求重点掌握启普发生器的使用以及气体相对分子质量的测定)
三、课前准备
1. 启普发生器的工作原理和使用方法:
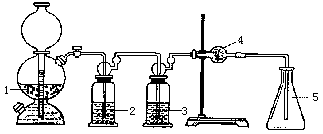
1——石灰石+稀盐酸
2——CuSO4溶液
3——NaHCO3溶液ss
4——无水CaCl2
5——磨口锥形瓶
2. 测定CO2相对分子质量
1)理想气体状态方程是:pV=nRT
2)同温同压下,同体积的两种气体满足:

◆小牛试刀
问题一:导入收集二氧化碳瓶中的导气管为何必须插入瓶底?怎样判断瓶内二氧化碳已收满?
问题二:为什么二氧化碳气体+瓶+塞的总质量要在分析天平上称量,而水+瓶+塞的质量可以在台秤上称量?两者的要求有何不同?
问题三:哪些物质可用此法测定相对分子质量?哪些不可以?为什么?
答案:
问题一:因为二氧化碳气体的相对密度大于空气,所以必须把导气管插入瓶底,才能把瓶内的空气赶尽。将燃着的火柴放于锥形瓶口,如果火焰熄灭,证明 CO2已充满。
问题二:这是因为二氧化碳气体的质量很小,在台秤上称量会因为精确度低而造成较大的误差,而水的质量相比较就大一些,在台秤上称量也不会造成很大的误差。两者的要求不同就是对精确度要求不同。
问题三:理论上来说只要比空气重的、容易净化和收集的气体都可以的,比如二氧化碳、氯化氢、氯气、二氧化硫等气体。但像一氧化碳、氢气和氧气等相对分子量比空气小或相差不大的气体,用排空气法收集很难得到纯净的气体,所以不能用相对密度法来测定它们的相对分子质量。
◆知识结构
 1. 电子天平的使用
1. 电子天平的使用
 2. 启普发生器的使用
2. 启普发生器的使用
 3. CO2相对分子量的计算
3. CO2相对分子量的计算

