第九章 电位分析法
 知识点二:离子选择性电极的特性参数
知识点二:离子选择性电极的特性参数
一、能斯特响应
离子选择性电极具有将溶液中某种特定离子活度变化服从于能斯特方程式,则称为能斯特响应。在此种情况下,对阳离子有响应的电极的膜电位为
![]() (9-18)
(9-18)
若待测离子是阴离子,膜电位为
![]() (9-19)
(9-19)
上二式中,K为常数,但不同的电极,K值不同,它与敏感膜、内部溶液组成等有关。在一定条件下,离子选择性电极的膜电位与测定离子活度的对数呈线性关系,这是离子选择性电极发测定离子活度的基础。
二、线性范围与检测下限
图9-9是以电极电位E对 作图所得的曲线。此曲线的直线部分(AB段)称为离子选择性电极响应的线性范围。在实际测定过程中,离子选择性电极电位值的变化随着被测离子活度的降低而逐渐变小,开始偏离能斯特方程。但当被测离子活度小到一定值以后,电极电位的变化越来越小,直至无电位变化为止,如图9-8CD所示。根据IUPAC推荐,离子选择性电极的检测下限为标准曲线延长部分与曲线直线部分切线的交点所对应的活度(或浓度)。
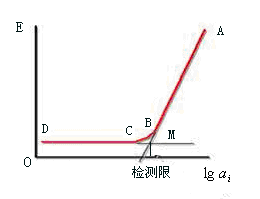
图9-9 电极标准曲线和检测下限
三、电位选择性系数
理想的离子选择性电极应只对某一种特定的离子产生电位响应,但事实上,任何一种离子选择性电极不可能作到这一点,在某种程度上它还会受到干扰离子的影响。一般情况下,试液中除了含有电极主要响应的离子i外,尚含有干扰离子j;为了表示干扰离子j对电位的贡献,可应用一个更为普遍适用的能斯特方程式,即
![]() (9-20)
(9-20)
式中 , 分别为待测离子和干扰离子的活度;ni,nj分别为i离子和j离子电荷数;式中右端第一项对阳离子为+号,对阴离子为-号。式中的Ki,j为干扰离子对待测离子的选择性系数。它可以理解为在其它条件相同时,提供相同电位所需待测离子活度 和干扰离子活度 的比值,即
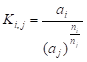 (9-21)
(9-21)
Ki,j常用来判断离子选择性电极对某种离子选择性的好坏。对于任何一种离子选择性电极来说,Ki,j值越小越好,它是离子选择性电极的最重要的特性参数之一。
借助于电位选择性系数Ki,j,可以粗略地估计某种干扰离子对待测离子在测量时产生的误差,以此判断在干扰离子存在下所用的测定方法是否可行。可用下式估计测定时的相对百分误差
相对误差(%)= ![]() (9-22)
(9-22)
例:硝酸根离子选择性电极对硫酸根离子的Ki,j为 。在1mol·L-1Na2SO4介质中测定8.2◊10-4mol·L-1硝酸根,由硫酸根引起的相对误差为多少?
解: 相对误差(%)=![]()
应该注意,Ki,j并非常数,它与i及j离子活度和实验条件及测定方法等有关。
四、响应时间
根据IUPAC的推荐,离子选择性电极的响应时间是指从离子选择性电极和参比电极一起接触试液时算起(或由试液中被测物质的浓度发生改变时算起),到电极电位达稳定值的某一瞬间所经过的时间。事实上,这一时间包括了离子选择性电极的膜电位平衡时间,参比电极的稳定时间及液接电位的稳定时间。
响应时间与待测离子达到电极表面的速度、活度、介质的离子强度等因素有关。响应时间是离子选择性电极在实际应用中的一个重要参数。
