第七章 质谱分析法
 知识点三:质谱分析法应用
知识点三:质谱分析法应用
质谱是纯物质鉴定的最有力工具之一,其中包括相对分子量测定、化学式确定及结构鉴定等。
一.相对分子质量的测定
利用质谱图上分子离子峰的m/z可以准确的确定该化合物的相对分子质量。一般说来,除同位素峰外,分子离子峰一定是质谱图上质量数最大的峰,它应该位于质谱图的最右端。但是,由于有些化合物的分子离子峰稳定性较差,分子离子峰很弱或不存在,给正确识别分子离子峰带来困难。因此,在判断分子离子峰时应注意以下问题。
(一)分子离子稳定性的一般规律
分子离子的稳定性与分子结构有关。碳数较多,碳链较长(有例外)和有支链的分子,分裂几率较高,其分子离子峰的稳定性较低;具有键的芳香族化合物和共轭链烯的分子离子稳定,分子离子峰大。
(二)分子离子峰必须符合氮规律
在只含有C、H、O、N的化合物中,含有偶数个(包括零)氮组成的化合物,其相对分子质量必为偶数;含有奇数个氮原子的化合物的相对分子量为奇数。这是因为在由C、H、O、N、S、P卤素等元素组成的化合物中,只有氮原子的化合价为奇数而质量数为偶数。这个规律称为“氮律”。不符合“氮律”的离子峰一定不是分子离子峰。
(三)利用碎片峰的合理性判断分子离子峰
在离子源中,化合物分子电离后,分子离子可以裂解出游离基或中性分子等碎片。若裂解出一个•H或•CH3、H20、C2H4碎片,对应的碎片峰为M-1、M-15、M-18、M-28等,这叫做存在合理的碎片峰。若出现M-3至M-14,M-21至M-25范围内的碎片峰,称为不合理碎片峰,则说明分子离子峰的判断有错。表明试样中可能存在杂质或者把碎片峰错误判断为分子离子峰。表7-2中列出从分子离子中裂解的常见碎片。
表7-2 从分子离子中裂解的常见碎片
碎片峰 |
游离基或中性分子碎片 |
碎片峰 |
游离基或中性分子碎片 |
M-1 |
•H |
M-33 |
(•CH3+H2O),HS• |
M-2 |
H2 |
M-34 |
H2S |
M-15 |
•CH3 |
M-41 |
C3H5• |
M-16 |
NH2,O |
M-42 |
CH2CO,C3H6 |
M-17 |
•OH,NH3 |
M-43 |
C3H7•,CH3CO• |
M-18 |
H2O |
M-44 |
CO2,C3H8 |
M-19 |
F |
M-45 |
•CO2H,•OC2H5 |
M-20 |
HF |
M-46 |
C2H5OH,NO2 |
M-26 |
C2H2,•CN |
M-48 |
SO,CH3SH |
M-27 |
HCN |
M-55 |
•C4H7 |
M-28 |
CO,C2H4 |
M-56 |
C4H8 |
M-29 |
•CHO,C2H5• |
M-57 |
•C4H9,C2H5CO• |
M-30 |
CH2O,NO |
M-58 |
C4H10 |
M-31 |
•OCH3,•CH2OH |
M-60 |
CH3COOH,C3H7OH |
M-32 |
CH3OH,S |
M-70 |
C5H10 |
(四)利用同位素峰识别分子离子峰
有些元素如35Cl、79Br、32S的同位素37Cl、81Br、34S相对丰度较大,其M+2同位素峰十分明显,通过M、M+2等质谱峰来推断分子离子峰,若分子中含一个氯原子时,M峰与M+2峰的强度比为3:1;若分子中含一个溴原子时,M峰与M+2峰强度比为1:1,这是因为M峰与M+2同位素峰强度比与分子中同位素种类、丰度有关。总之,同位素离子峰的信息有助于分子离子峰的正确判断。
(五)由分子离子峰强度变化判断分子离子峰
在电子轰击离子源(EI)中,适当降低电子轰击电压,分子离子裂解减少、碎片离子减少,则分子离子峰的强度应该增加;在上述措施下,若峰强度不增加,说明不是分子离子峰。逐步降低电子轰击电压,仔细观察m/z最大峰是否在所有离子峰中子后消失,若最后消失即为分子离子峰。
二.化学式的确定
用质谱法确定有机化合物的化学式,一般是通过同位素峰相对强度法来确定。各元素具有一定天然丰度的同位素(见表7-1),从质谱图上测得分子离子峰M、同位素峰M+1和M+2的强度,并计算其(M+1)/M、(M+2)/M强度百分比,根据拜诺(Beynon J H)质谱数据表查出可能的化学式,再结合其他规律,确定化合物的化学式。
例1:某化合物的质谱数据如下,试确定该化合物的化学式。
m/z M(150) M+1(151) M+2(152)
与M强度比/% 100 9.9 0.9
解:由M+•(M)的质量数,可知此化合物的相对分子质量为150。M+2峰的强度百分比为0.9%,由表7-1可知,该化合物不含Cl、Br、S。查阅拜诺表可知,相对分子质量为150的化学式共有29个,其中M+1峰的强度百分比在9%~11%的化学式有如下7种:
化学式 (M+1)/M/% (M+2)/M/%
①C7H10N4 9.25 0.38
②C8H8NO2 9.23 0.78
③C8H10N2O 9.61 0.61
④C8H12N3 9.98 0.45
⑤C9H10O2 9.96 0.84
⑥C9H12NO 10.34 0.68
⑦C9H14N2 10.71 0.52
此化合物相对分子质量为偶数,根据氮规律,应该排除②、④、⑥三个化学式;在剩下的四个化学式中,⑤化学式的M+1峰的强度百分比与9.9%最接近,M+2峰的强度百分比与0.9%也最接近。因此,该化合物的化学式应该是C9H10O2。
三.结构式的确定
在确定了未知化合物的相对分子质量和化学式以后,首先根据化学式计算该化合物的不饱和度,确定化合物化学式中双键和环的数目。然后,应该着重分析碎片离子峰、重排离子峰和亚稳离子峰,确定分子断裂方式,提出未知化合物结构单元和可能的结构。最后再用全部质谱数据复核结果。必要时应该考虑试样来源、物理化学性质以及红外、紫外、核磁共振等分析方法的波谱信息,确定未知化合物的结构式。
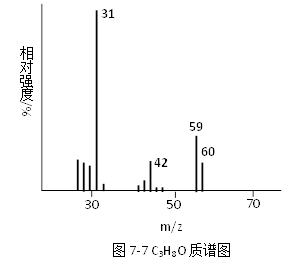
例2:某化合物分子式为C3H8O,其质谱图如图7-7所示。红外光谱数据表明在3640cm-1和1065~1015cm-1有尖而强的吸收峰,试解析该化合物的分子结构。
解:分子的不饱和度为 ![]()
说明化合物分子内的化学键皆是单键。在3640cm-1及1065~1015cm-1有强红外吸收峰,表明化合物属醇类。
由质谱图可知,m/z 60峰是分子离子峰,该化合物的相对分子质量为60。
由于m/z 59峰的出现,可能发生下述裂解:![]()
m/z 60 m/z 59
m/z 42峰是由分子离子峰失去中性碎片H2O而生成的,其裂解反应的机理如下:
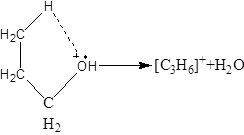
m/z 60 m/z 42
反应中有亚稳离子生成,m*=422/60=29.4,这与质谱图中的亚稳离子峰的位置相符合。
基峰m/z 31是CHO+H碎片离子峰,断裂的机理为:
![]()
m/z 60 m/z 31
因此,该化合物为正丙醇,结构式为CH3-CH2-CH2-OH。
四.质谱定量分析
(一)无机痕量分析
火花源质谱仪可以分析无机固体试样,它已成为金属、合金、矿石和超导体中痕量元素分析的重要方法。通过离子峰相对强度的测量可进行质谱定量分析。该方法的特点是灵敏度高,对元素的检出限约为纳克每克数量级(ng/g)。由于质谱图简单,并且各元素峰强度大致相当,应用很方便。
(二)同位素的测定
质谱定量分析最早用于同位素丰度的研究。稳定的同位素可以用来“标记”各种化合物,例如确定氘苯C6D6的纯度,通常可用C6D6+与C6D5H+、C6D4H2+等分子离子峰的相对强度进行定量分析。在考古学和矿物学研究中,应用同位素比测量法来确定岩石、化石和矿物年代。
(三)混合物中的定量分析
混合物的质谱定量分析,目前常用于多组分气体和石油中挥发性烷烃的分析。通过计算机求解数个联立方程,得到各组分的含量。该方法一次进样实现全分析,快速、灵敏。
