第五章 红外光谱法
 知识点一:红外吸收的基本原理
知识点一:红外吸收的基本原理
红外吸收光谱法(Infrared Absorption Spectrometry,IR)简称红外光谱法。当分子在红外光范围内的电磁场中接受一定的辐射能量,即光的频率与分子中基团的能级相同时,就发生共振,产生分子对红外光的选择性吸收,呈现相应的红外吸收光谱。
红外光谱法不仅能进行定性和定量分析,而且从分子的特征吸收可以鉴定化合物和分子结构。
一、分子的振动
(一)谐振子
分子振动原子以平衡点为中心,以非常小的振幅作周期性的振动,可近似地看作简谐振动。这种分子振动模型,以经典力学的方法可把两个质量为m1和m2的原子看作刚体小球,连接两原子的化学键设想成无质量的弹簧,簧的长度r就是分子化学键的长度(图5-1)。
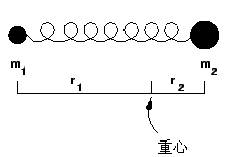
图5-1 谐振子振动示意图
由经典力学可导出该体系的基本振动频率计算公式
![]() (5-1)或
(5-1)或
![]() (5-2)
(5-2)
式中k为化学键的力常数,其定义为将两原子由平衡位置伸长至单位长度时的恢复力(单位为N • cm1),单键、双键和三键的力常数分别近似为5、10和15 N • cm1;c为光速,2.998×1010 cm · s-1;为折合质量,单位为g,且
![]() (5-3)
(5-3)
根据小球的质量和相对原子质量之间的关系,式可写为
![]() (5-4)
(5-4)
N是阿伏伽德罗常数(6.002×1021 mol-1),M是折合原子质量,如两原子的相对原子质量分别为M1和M2,即
![]() (5-5)
(5-5)
式(5-2)或(5-4)为分子振动方程式。
从式(5-4)可见,影响基本振动频率的直接因素是相对原子质量和化学键的力常数。力常数越大,折合相对原子质量越小,化学键的振动频率越高,吸收峰将出现在高波数区;反之,则出现在低波数区。
(二)非谐振子
实际上双原子分子并非理想的谐振子,比较双原子分子与谐振子的振动位能曲线如图5-2所示。
在低能量时,两条曲线大致吻合,可以用谐振子模型来描述实际位能。曲线左侧,实际位能曲线高于谐振子位能。原因是两原子间距离较近时,核间存在库仑排斥力(与恢复力同方向),使位能值大。高位能区,位能间距变小,因此Δν ≠ 1的跃迁成为可能。
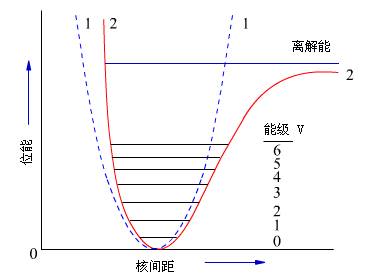
图5-2 双原子分子振动位能比较
1. 谐振子振动位能曲线;2.双原子分子振动位能曲线
(三)分子的振动形式
构成分子的原子不是静止不动的,原子在其平衡位置做相对运动,从而产生振动或转动,原子与原子之间的相对运动有两种情况,一种是键长发生变化(伸缩振动),另一种是键角发生变化(弯曲振动)。多原子分子由于组成原子数目增多,组成分子的键或基团和空间结构的不同,其振动光谱比双原子分子要复杂得多。
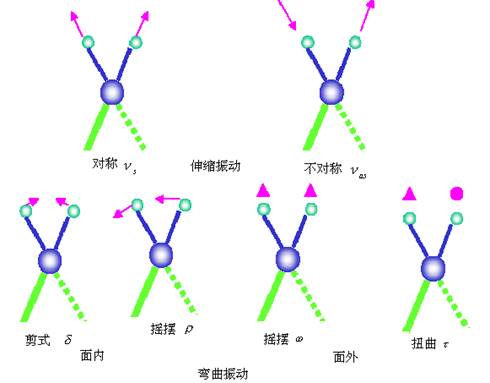
(1)伸缩振动
原子沿键轴方向伸缩,键长发生变化而键角不变化的振动称为伸缩振动。它又可分为对称伸缩振动(νs)和不对称伸缩振动(νas)。对同一基团来说不对称伸缩振动频率要稍高于对称伸缩振动。
(2)弯曲振动(变形振动或变角振动)
基团键角发生周期性变化而键长不变的振动。变形振动又分为面内变形和面外变形振动。面内变形又分为剪式(以δ表示)和平面摇摆振动(ρ)。面外变形振动又分为非平面摇摆(ω)和扭曲振动(τ)。
(四)振动自由度
多原子分子简正振动的数目称为振动自由度,每个振动自由度相应于红外光谱图上一个基频吸收。三维空间中,每个原子都能沿x、y、z三个坐标方向独立运动。对于n个原子组成的分子则有3n个独立运动,即3n个运动自由度。但是这些原子由化学键链接为一个整体,分子作为整体的运动状态可以分为三类:平动、转动和振动。由于分子重心向任何方向的移动都可以分解为沿三个坐标方向的移动,因此,分子有三个平动自由度。在非线性分子中,整个分子可以绕三个坐标轴转动,故也有三个转动自由度。 剩下的3n- 6个才是振动自由度。对于直线性分子,若键轴是在x方向上,整个分子只能绕y、z轴转动,故振动自由度为3n-5。
例如,水是一个非线性分子,振动自由度为3×3-6 = 3, 即有三种振动形式。
νs:3625 cm-1 νas :3756 cm-1 :1595 cm-1
CO2是线性分子,振动自由度为3×3-5 = 4,它具有四种基本振动模式。CO2中的对称伸展并不引起偶极矩的变化,因此它是红外非活性的。另外三种模式则是红外有活性的。
νs:1338 cm-1 νas:2349 cm-1
δ:667 cm-1 τ:667 cm-1
二、红外吸收光谱产生的条件和谱带强度
(一)分子吸收红外辐射的条件
分子的每一个基本振动都对应于一定的振动频率,但并不是每一种振动都对应有吸收谱带,分子吸收红外辐射必须同时满足以下两个条件。
1、辐射光具有的能量与发生振动跃迁所需的能量相等
以双原子分子的纯振动光谱为例,双原子分子可近似看作谐振子。根据量子力学其振动能量Eν是量子化的
![]() (5-6)
(5-6)
式中为分子振动频率;h为Planck常数;v为振动量子数,v=0,1,2,3,,分子中不同振动能级的能量差ΔEv= Δvhν。吸收光子的能量hva必须恰等于该能量差,因此
![]() (5-7)
(5-7)
在常温下绝大多数分子处于基态(v=0),由基态跃迁到第一振动激发态(v=1)所产生的吸收谱带称为基频谱带。因为Δv=1,因此
![]() (5-8)
(5-8)
也就是说,基频谱带的频率与分子振动频率相等。
2、只有能使偶极矩发生变化的振动形式才能吸收红外辐射
分子由于构成它的各原子电负性不同,显示不同的极性,称为偶极子。通常用分子的偶极矩(μ)来描述分子极性的大小。当偶极子处在电磁辐射的电场中时,该电场作周期性反转,偶极子将受交替的作用力而使偶极矩增加或减少。由于偶极子具有一定的原有振动频率,显然,只有当辐射频率与偶极子频率相匹配时,分子才能与辐射相互作用(振动耦合)而增加它的振动能,使振幅增大,即分子由原来的基态振动跃迁到较高的振动能级。因此,并非所有的振动都会产生红外光谱,只有偶矩发生变化(Δμ ≠ 0)的振动才能引起可观测的红外吸收光谱,该分子称为红外活性的。Δμ = 0分子振动不能产生红外振动吸收,称为红外非活性的。
实际观察到的红外吸收峰数目并不等于振动自由度。其原因除了上面讨论的有些振动是非红外活性的,不产生吸收外,还有以下几种原因:(1)由于对称的缘故,有些振动的频率相同,因而发生简并,只有一个吸收峰,如CO2的面内及面外弯曲振动;(2)有些吸收峰特别弱或彼此十分接近,仪器检测不出或分辨不出;(3)有些吸收峰落在仪器检测范围之外。此外,由于振动之间的相互作用还会产生组频峰(包括和频峰ν1 + ν2、2ν1 + ν2和差频峰ν1- ν2 , 2ν1 - ν2)。倍频峰、组频峰(统称泛频峰)的存在,又可以产生一些附加的吸收峰。不过泛频峰一般都很弱。
二、吸收谱带的强度及其影响因素
分子振动时偶极矩是否发生变化决定了该分子能否产生红外吸收,而偶极矩变化的大小又决定了吸收谱带的强弱。
在红外吸收光谱定性分析中,根据摩尔吸收系数ε的大小,通常把谱带的强度分为:ε > 100 ,极强(vs);20 < ε <100,强(s);10< ε <20,中(m);
1< ε < 10,弱(w);ε < 1,极弱。
影响吸收谱带强度的因素大致有以下几种:
1、跃迁几率
(1)从基态向第一激发态跃迁,几率大:基频峰一般较强,而倍频峰一般较弱;
(2)对于基频峰:偶极矩变化越大的振动,吸收峰越强。
2、偶极矩的变化值
(1)原子的电负性相差越大,即键的极性越大,偶极矩变化越大:C-Cl比C-H强;
(2)分子的对称性:越差,偶极矩变化越大;对称性分子没有红外活性。
如:ClCH=CCl2,有C=C峰;而Cl2C=CCl2无C=C峰;
(3)一般来说,不对称伸缩>对称伸缩,伸缩>弯曲。
